oli juhus – katse-eksituse meetod. Hiljem: avastati järjesti uusi signaalmolekule ning need juhatasid sihtmärkideni. Enamik virgatsaineid on tänaseni tundmata, kuna kontsid on liiga madalad või aine liig lühikese elueaga. Seetõttu püsisid ka potentsiaalsed ravimi sihtmärgid varjus. Täna: molekulaarbioloogia edusammud tegid olukorra vastupidiseks. Geeniprojektid andsid tohutu infopanga uute ensüümide ja retseptorite kohta, mis on potentsiaalsed ravimi sihtmärgid. Nüüd on medkeemia ülesandeks leida keemilised ühendid, mis nende sihtmärkidega interakteeruksid, määramaks nende bioloogilised funktsioonid ja otsustamaks nende sobivust olema ravimi sihtmärgiks. MIDA SUUREM ON RAVIMI SELEKTIIVSUS ÜHE KITSA SIHTMÄRGI SUHTES, SEDA VÄIKSEM ON TÕENÄOSUS INTERAKTSIOONIDEKS TEISTE SIHTMÄRKIDEGA JA SOOVIMATUTEKS KÕRVALNÄHTUDEKS. N: antimikroobsetest agentidest parimatel ei leidu inimorganismis sihtmärke, küll aga mikroobis
Kordamisküsimused I Loeng 1 Mis on meditsiiniline keemia ja mida uurib? Meditsiiniline keemia on keemiline distsipliin, mis hõlmab füsioloogia, mikrobioloogia, rakubioloogia, farmakoloogia ja farmaatsia aspekte. Distsipliini eesmärk on uute bioloogiliselt aktiivsete ühendite avastamine, identifitseerimine ja süntees, metabolismiuuringud, toimemehhanismide välja selgitamine molekulaartasandil, struktuur-aktiivsus uuringud, ravimidisain struktuuri ja farmakokineetika seisukohast. Mis on ravim? Ravim on iga valmistatud, turustatud või turustamiseks määratud aine, mis on ette nähtud haigete ravimiseks, haigusseisundi kergendamiseks, haiguste ärahoidmiseks või diagnoosimiseks inimesel või loomal, inimese või looma elutalitluse taastamiseks, korrigeerimiseks või muutmiseks (WHO). Ravimisarnasel ainel on toimeainet koguses või vormis, mis ei luba teda pidada ravimiks, või mis ei sisalda üldse toimeainet, kuigi tootja kirjeldab tootel ravimile isel
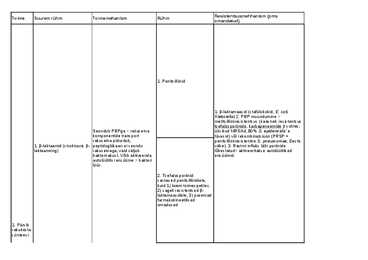
preparaatide rühm toimemehhanism resistentsuse mehhanismid esindajad toimespekter β-laktaamsed • Antibiootikum seostub • β-laktamaaside produktsioon penitsilliinid naturaalsed kõik streptokokid, meningkokid, enamik G+ antibioootikumid penitsilliini siduva proteiiniga nii G- kui G+ mikroobidel anaeroobe. minimaalne aktiivsus stafülokokkide (bakteritsiidsed) (PBP) (plasmiidne DNA, G- suhtes • Peptidoglükaani süntees
Üldine osa Mikroorganismide ehitus ja elutegevus § Mikrobioloogia on teadus, mis uurib väikseimate elusorganismide mikroorganismide morfoloogiat, füsioloogiat, biokeemiat ja geneetikat, seega mikroobide mitmesuguseid omadusi. Kihn § Nimetatakse veel: glükokaaliks, limakiht, kihn. § Ei esine kõigil bakteritel, varieerub paksuses ja rigiidsuses. § Tagab bakteri adhesioonivõime, väldib fagotsütoosi. § Paljud bakterid kaotavad kunstlikel söötmetel kihnu. Bakterite rakusein § Mükoplasmad on ainukesed bakterid, kellel rakusein puudub. § Bakterite (v.a. klamüüdia) rakusein on poolrigiidne, sisaldades peptidoglükaani [PG] (mureiini). § PG tagab bakterite kuju ja takistab osmoosist tingitud lüüsi. Tsütoplasma membraan § Tegemist on permeaabelsusbarjääriga, määrates, mis liigub sisse ja mis välja. § Vesi, lahustuvad gaasid (CO2, O2), rasvlahustuvad molekulid difundeeruvad läbi membraani, vesilahustuvad väikese
1. Bakterirakus leiduvad polümeraasid: ! Replikatsiooni viivad läbi DNA polümeraasid (erinevad eri ahelatel). Replikatsioonijärgne parandamine: polümeraasid. Valepaardumiste eemaldamiseks: DNA polümeraas III – lisab nukleotiide sünteesitava ahela 3’ otsa; suudab eemaldada viimase DNA-le lisatud nukleotiidi (eksonukleaasne aktiivsus) st valesti lisatud nukleotiid eemaldatakse ning asendatakse õigega: DNA üks parandusmehhanisme bakteris. Pärast vea eemaldamist replikatsioon jätkub. DNA polümeraas I – aeglasem, aga tal on nii 3’ 5’ kui ka 5’ 3’ eksonukleaasne aktiivsus; Replikatsiooni käigus tunneb ära RNA praimeri ja asendab selle desoksüribonukleotiididega; Parandab vead, mida ei suutnud parandada DNA polümeraas III On ka DNA polümeraas V ja IV – neil puudub 3’-5’ eksonukleaasne aktiivsus, seetõttu teevad nad palju vigu 2. PRO- JA EUKARÜOOTSE RAKU GENOOM
RAVIM Kineetika & dünaamika Toimemehhanism Kasutus ja kõrvaltoimed N-KOLINOMIMEETIKUMID Atsetüülkoliin (M ja N) Ei läbi HEBi ega PBd Laialdane toime üle kogu organismi, kiire Ei kasutata meditsiiniliselt Laguneb GI-s, mõttetu manustada lammutumine ACh-esteraasi toimel, N- ja I.v. toime tugev, lühiajaline M-kolinomimeetikum Retseptorid Nn ganglionides, Nm neuromuskulaarsel lõpp-plaadil, M1-KNS, M2-süda, M3-näärmed, silelihased, veresooned
Resistentsusmehhanism (pms Toime Suurem rühm Toimemehanism Rühm omandatud) 1. Penitsilliinid 1. -laktamaasid (stafülokokid, E. coli, Klebsiella) 2. PBP muundumine > metitsilliiniresistentsus (kaasneb resistentsus tsefalosporiinide, karbapene
”Rakubioloogia II” aineprogramm. DNA struktuur ja funktsioonid. Nukleotiidide koostisosad (lämmastikalused, suhkur, fosfaatgrupp). Lämmastikalused puriinid:adeniin,guaniin 2-tsüklilised Lämmastikalused pürimidiinid:uratsiil, tümiin, tsütosiin- ühetsüklilised Suhkur:pentoos-riboos või desoksüriboos Nukleosiid: alus + suhkur (dAMP,dGMP) Nukleotiid: alus 1´ + suhkur + fosfaatgrupp 5´ Keemilised sidemed DNA kaksikheeliksis. Nukleiinhappe teke: fosfodiester sidemetega ühendatud 5´algus 3´ lõpp süsinikega. Uus nukleotiid lisatakse 3´otsa. Nukleotiidide vahel on vesinikside DNA polünukleotiidisete üksikahelate keemiline polaarsus. DNA kaksikahelas olevate polünukleotiidide vastassuunalisus e. Antiparalleelsus- kaksikahel, üks kulgeb 5´3´ ja teine 3´5´ Nukleotiidide komplementaarsuse printsiip- lämmastikaluste võime omavahel seonduda jamoodustada paar A=T(U), G=C DNA kaksikheeliksi suur ja väike vagu- suur vagu 3,4nm, sisaldab 10 nukleotiidi ning vahem







Kõik kommentaarid